

●宮崎医科大学 医学部化学 中島 暉
微量の重金属イオンは、生物体にとって必須のものであるが、過剰に存在すると有害になる。
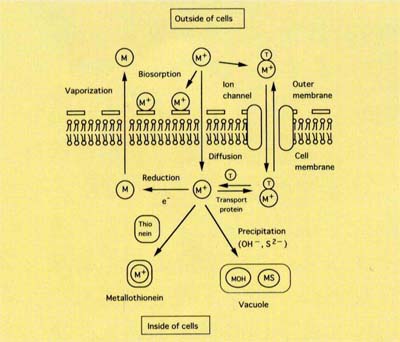
ある種の微生物では、有害金属に対する防御機構を持つものがあり、(1)膜を介するイオンポンプにより細胞外へ排出する、
(2)化学反応により無害化して揮発するかまたは液胞へ蓄積する、(3)細胞物質に結合させて無害な形で隔離するなどの方法をとっている(図1)。
これらのうち、(3)には、誘導タンパクと結合してメタロチオネインを形成する場合と代謝と無関係に細胞物質に結合する生物吸着(Biosorption)とがある。
この生物吸着は細胞外部に重金属を蓄積し、しかも蓄積容量が大きいことから、生体による有害金属防御機構の解明だけでなく、
水圏中有用金属資源の回収及び環境中有害重金属元素の制御の視点からも、近年、活発に研究されている。筆者は、毒性元素の一つである銅に注目し、
細菌による銅生物吸着の機構を解析している。ここでは、これまでに明らかになったことを紹介する。
細菌による銅吸着特性は、菌体中銅を中性子放射化分析法で定量し解析している。
図2に、日本原子力研究所JRR-4炉気送管で中性子照射した細菌粉末のγ線スペクトルを示す。
1039.0KeV(66Cu,半減期5.10min)及び1345.5KeV(64Cu,半減期12.8h)
のγ線強度からµgオーダーの銅を定量することが出来る。細菌類は概して優れた銅吸着能を持っており、Arthrobacter菌は、
菌体1g当たりに586µmol(1.18mEq/g)の銅を吸着することができる(表1)。該菌による銅吸着は、(1)溶液のpHの影響を受け、pH5〜6で最大の吸着量を示す、
(2)吸着速度はきわめて速く、銅溶液接触後、10分で吸着平衡に達する、(3)Langmuirの吸着等温式に従うなどの特性を持っている。
これらの結果は、細菌類の銅吸着が代謝と無関係な生物吸着であることを示唆している。
細菌菌体に吸着した銅の微視的状態は、ESR分析法により解析を行っている。
細菌菌体に吸着された銅(?U)イオンのESRパラメーター(G〃‚|A〃|α2)を表1に示す。
g〃と|A〃|の関係を銅蛋白質のデータと併せてプロットすると図3のようになる。
ここで、4N、2N2O、4Oなどは、正方構造の4つの配位原子を表す。
この図から、細菌菌体に吸着した銅(?U)イオンは、Type?Uの銅タンパク質と同様、2N2Oの配位原子を持つことがわかる。
また、酸性(pH3)溶液から吸着した銅(?U)イオンのg〃と|A〃|の関係は、
図3で40側にシフトし、アミノ酸化学種のpH変化と対応する。
さらに、Kivelsonの式から求めたd軌道上の不対電子密度α2の値は、0.82〜0.85で、通常の銅錯体の値(0.7〜0.9)の範囲内である。
これらの結果から、細菌菌体中の銅(?U)イオンは、細胞内タンパク質アミノ酸残基の窒素原子及び酸素原子に結合した正方構造(歪んだ正八面体構造)をもつと考えられる。
 |
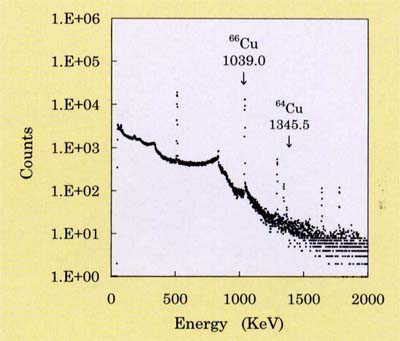 |
| 図1.生物体による重金属元素排除機構 | 図2.中性子照射細菌粉末のγ線スペクトル |
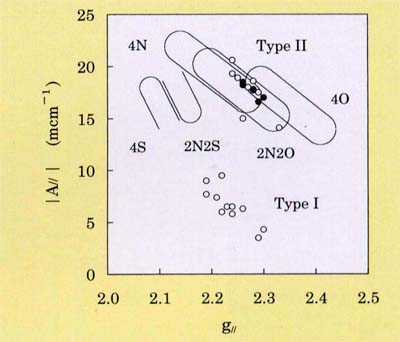 |
| 図3.細菌菌体中銅(?U)のg〃と|A〃|の関係 (●:細菌-銅(?U)、○:銅タンパク質) |
表1.細胞による銅の吸着量及び菌体中銅(?U)のESRパラメーター
| 菌種 | Cu吸着量 | ESRパラメーター | |||
| % | µmol/g | g〃 | |A〃|mcm-1 | α2 | |
| Arthrobacter nicotianae | 39.5 | 589 | 2.30 | 17.3 | 0.84 |
| 2.26 | 18.9 | 0.85 | |||
| Bacillus subtilis | 14.9 | 316 | 2.26 | 18.5 | 0.84 |
| Escherichia coli | 17.6 | 287 | 2.29 | 16.6 | 0.82 |
| Pseudomonas stutzeri | 26.8 | 404 | 2.26 | 18.5 | 0.84 |
| Micrococcus luteus | 20.2 | 337 | 2.30 | 17.0 | 0.84 |
| Zooglea ramigera | 18.0 | 303 | 2.26 | 18.3 | 0.83 |
Kivelsonの式:α2=-(A〃/P)+(g〃-ge)+(3/7) (g⊥-ge)+0.04 (P=3.6×10-2cm-1)